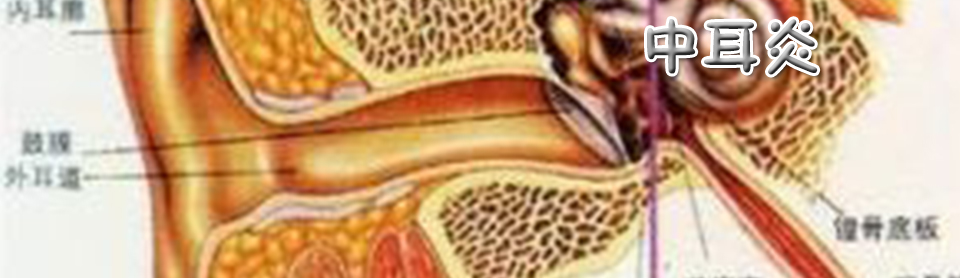
专家视点儿童分泌性中耳炎治疗国际共识
关键词:儿童分泌性中耳炎
最新的世界耳鼻咽喉科学联合会(IFOS)国际共识(巴黎)中,将无任何耳部感染迹象的中耳积液称为分泌性中耳炎(OME)。OME是儿童非常常见的疾病,儿童的咽鼓管功能较成人差,阻碍了中耳的通气,并最终导致了OME的高发病率。OME在年龄较大的儿童中常可自然治愈并不易复发。OME病史过长可最终导致鼓膜形成内陷袋,鼓膜不张,继而形成胆脂瘤。一些研究强调了炎症反应机制在OME发病的作用,包括鼓室积液中发现了细菌及病毒感染的迹象。污染、过敏、胃食管返流及遗传等危险因素亦被证实。然而,目前仍然很难从现有的这些结果中得出强有力的因果推断。
与OME诊断相关的具体评估胃食管反流疾病和过敏
01
OME诊疗的第一步应进行全方面的临床检查及评估。可通过鼓气耳镜和鼓室图明确诊断。慢性OME定义为持续监测3个月以上仍有中耳积液(A级证据)[1]。持续性鼻塞或单侧长期分泌性中耳炎可使用鼻内镜检查是否有腺样体肥大(C级)[1]。在艾滋病高发地区应更加常规使用鼻内镜检查以排除鼻咽部病变(淋巴瘤)[1]。与OME相关并且直接影响诊疗的高危因素是胃食管返流疾病(GERD)和过敏。中耳积液中发现胃蛋白酶和幽门螺杆菌提示GERD与OME相关,但因果关系尚未被证实。也没有任何研究令人信服地证明治疗GERD将改善或治愈OME[1]。
研究还表明过敏与OME之间存在关联,如果儿童出现如慢性鼻炎、鼻甲肿大、哮喘或过敏,有必要进行过敏评估(B级)[1]。另外,在某些空气质量差和污染问题严重的地区,即使对于较轻微的临床症状也应更系统地进行过敏评估(C级)[1]。虽然有证据表明过敏与OME之间存在关联,但尚缺乏令人信服证据证明治疗过敏会影响OME疗效(B级)[1]。共识认为,无相关症状儿童无需常规进行过敏或GERD评估。在某些特定情况下,如年长的孩子持续OME(超过七岁,咽鼓管功能障碍可能性较小),应该进一步评估最常见的风险因素,如GERD和一些罕见的鼻咽部梗阻因素。
听力检查
02
此次IFOS国际共识推荐听力测试为OME唯一需常规进行的检查。计算,,和赫兹的平均听阈(PTA),约有50%的OME患者听力损失20dB,20%听力损失超过35dB,5-10%的听力损失高达50dB。仅仅由OME造成的超过50dB的听力下降很少,这种情况通常伴有其他中耳或内耳病变[1]。在大多数国家,在听力相关手术前需要进行听力状态评估,尤其是一些儿童言语发育迟缓或各类综合征并发OME病例。
指南建议在植入鼓膜通气管之前进行听力测试。首先,它可以帮助外科医生明确手术指证,同时精确测量听力损伤程度来确认手术指证,也更加容易让父母接受。其次,进行感音神经性耳聋检测。检测手段根据年龄有所不同,3-4岁龄通常使用自由场,包括纯音测听,言语测听和骨传导测试。即使是自由场评估也不可能的情况(年龄太小),建议客观听觉检测,如听性脑干反应(ABR),以免遗漏相关的感音神经性听力损失(C级)。[1]
非手术治疗儿童OME是由于各种解剖学因素造成的(咽鼓管短,软和水平),这些因素加剧了由免疫反应等因素造成黏膜水肿所引起的后果。目前没有药物治疗或手术治疗可以直接解决这种功能障碍。因此,OME的非手术治疗的目标是通过无害且成本可控的方法限制中耳慢性炎症,直到随着孩子的成长咽鼓管功能达到正常。口腔或鼻腔使用类固醇、抗生素、抗组胺剂、减充血剂或粘液溶解剂和自动扩张技术等方法均已被应用。所有这些方法已经被研究并进行了Meta分析比较疗效,大多数缺乏对积液吸收或听力恢复的远期疗效。[1]
糖皮质激素
01
口服和鼻用糖皮质激素已被广泛用于减轻咽鼓管和中耳的炎症。在我国,使用鼻用糖皮质激素治疗分泌性中耳炎已经成为治疗常规,其中包括全身应用激素、鼻腔局部应用激素、雾化吸入激素、以及咽鼓管注射激素。但大多是根据临床经验用药,缺乏相关循证医学依据。这些单机构小样本的疗效研究大多缺乏严谨的实验设计,证据力度欠缺。涵盖了12项研究、例患者的国外研究显示糖皮质激素没有改善长期OME的临床症状[1]。虽然这些研究表明口服糖皮质激素可短期改善OME症状,但有如腹泻、恶心、多动和流鼻血等副作用。同样,局部应用糖皮质激素在解决OME症状包括短期听力损伤方面没有任何益处(A级)[1]。
总体上,该指南并不推荐使用糖皮质激素治疗,原因包括治疗成本,可能的副作用以及缺乏长期疗效。
抗生素
02
国内目前报道的分泌性中耳炎的治疗中,青霉素类、头孢类、大环内酯类抗生素均被用于治疗儿童分泌性中耳炎,但均为小样本且证据等级较低的研究,疗效与评价各自不同。美国版的儿童分泌性中耳炎诊治指南中,将抗生素列为强烈不推荐等级,认为抗生素在治疗儿童OME中并无明确疗效。我国儿童中耳炎临床指南中,也未将抗生素列入分泌性中耳炎的治疗措施中。最近的Cochrane评价包括了23项研究和例患者,比较抗生素连续治疗(主要是阿莫西林),时程从10天到6个月,结果未显示出对听力、鼓膜置管率或语言发育的影响(A级)[1]。生物膜假说帮助我们解释了为什么我们不应该期望全身应用低浓度抗生素到达中耳以根除感染。使用抗生素也会增加成本以及增加抗生素耐药性。
其他治疗
03
其他非手术治疗被证实疗效差或无效。OME与过敏有关,但是没有令人信服的证据表明治疗过敏(例如试图减少咽鼓管粘膜水肿)对OME具有任何效果。另一方面,1项涵盖了16项研究、例患者的Meta分析(A级)显示,减充血剂和抗组胺药可诱发副作用,并且没有显示出临床或统计学上的获益[1]。几项关于OME伴过敏患者的研究表明抗组胺药可以对过敏性鼻炎产生积极的作用,但对OME的任何影响可能源于其自然病程(A级)[1]。
粘液溶解剂减少中耳粘液产生,具有短期疗效。虽然长期疗效尚未经证实,粘液溶解剂可用于观察治疗期间用药,这些药物相对无害且便宜(B级)[1]。
咽鼓管吹张
04
国外研究发现2岁龄儿童经过四周的治疗后中耳压力和听力均有显着改善(B级)[1]。程雷等研究认为,利用改良Politzer仪进行咽鼓管吹张能有效治疗患儿慢性OME,越早吹张治疗效果越好,从而降低手术机率。这项治疗措施尚待改进之处在于需要开发标准化、便宜且易于使用的设备。咽鼓管吹张仪的价格仍相对较高,尤其是对收入水平不高的欠发达地区而言,在一定程度上限制了推广。
鼓膜通气管选择鼓膜通气管的时机
国际共识认为复发性急性中耳炎和听力损失是鼓膜置管的两个指征,与美国儿童分泌性中耳炎诊疗指南中推荐的鼓膜置管指征一致。关于复发性急性中耳炎,目前尚无正式的关于严重性或发作频率的标准,但传统的指南定义为6个月之内发作≥3次或1年之内发作≥4次的标准已广泛用于临床指导。关于听力损失的标准,不同的国家标准从25dB至40dB不等。国际共识认为儿童听力损失的评估应结合各方面因素而非单纯依赖纯音测听。例如,一个孩子可能在25dB的听力损失时就会遇到交流困难,而另一个在听力损失40dB时仍可以维持正常社交和学校生活。单次听力测试并不能反映可能的听力波动情况。共识认为,个体化治疗在鼓膜置管的决策中十分重要。
目前我国儿童中耳炎临床指南将病程3月推荐为鼓膜置管指征。
通气管种类的选择
01
最常用的短期管是Shepard管,国内多称为“纽扣管”。在欧洲,中国和南非最为常见,通常在六个月内脱落。Armstrong管(斜口型通风管)是北美地区使用的主要类型之一。通常在9-14个月时自动脱落。管型的选择必须根据个体的治疗策略。Armstrong管的较长留置时间可对应OME的自然病程,因此可对儿童带来更大的益处直到其咽鼓管功能正常。另一方面,Shepard管更适合于季节性OME,特别是与腺样体切除术相关联时。笔者的一项研究发现,儿童OME植入纽扣管后,脱管后OME的复发率高达31.21%,多集中在3-6岁儿童,提示纽扣管的自然脱管时间对于中国儿童OME的痊愈仍显不足。推荐3-6岁,尤其是伴有变应性鼻炎的患儿初次鼓膜置管时采用T型管,留置时间适当延长至13个月以上,年龄越小留置时间越长,避开发病高峰;6岁以上的患者可采用纽扣型管,待其自然脱落[9]。
诸如硅胶T管之类的长期管不能自然脱落,通常放置2年,一般用于复发型OME患者第一次使用Shepard管后。T管与短期通风管相比,穿孔的相对风险增加3.5倍,胆脂瘤风险增加2.6倍(A级),有不同程度耳漏的风险(A级)[1]。T型管导致穿孔的风险很高,在一项荟萃分析中达到16%(A级),其他最近的研究则为1-6%(A级)[1]。笔者研究显示儿童OME鼓膜置管术后并发症发生率为6.34%,包括耳溢液、急性化脓性中耳炎、中耳肉芽、鼓膜穿孔、耳鸣。使用长期或短期通风管应考虑到家庭原因以及病因,不仅要考虑到复发的可能性,还要考虑到随访的可能性。
对于鼓膜内陷的OME病例,国际共识认为短管或中间管应该是最好的选择以尽可能减少并发症。但在很多情况下,鼓膜完全内陷,缺乏足够的空间,则需要使用T型管。
耳漏的处理
02
耳漏是鼓膜通气管植入后最常见的并发症,可在3%至50%的病例中出现。没有证据表明避免耳道进水可防止这种情况的发生,更可能的原因是上呼吸道感染产生的鼻腔分泌物通过功能异常的咽鼓管到达中耳(A级)[1],或者通过外耳道引起的感染(非水暴露)。
不推荐使用口服抗生素治疗儿童鼓膜通气管植入后引起的耳漏,这与成本和副作用两个因素有关。首先,耳漏的主要病原菌为铜绿假单胞菌,对普通儿童使用的口服抗生素耐药。其次,通过通气管可以使用喹诺酮进行局部治疗。喹诺酮滴耳液可达到的局部药物浓度比口服抗生素高倍,这大大提高了疗效并减少了对细菌的耐药性。避免因耳漏取管,因为很容易导致OME复发。
通气管的疗效
03
OME造成的听力损失是进行鼓膜置管术的主要原因,已经有大量关于置管后短期和长期听力影响的相关研究。1项包括了10个随机对照研究的系统评价提示Shepard管有短期听力获益(增益为12dB)[1]。国外文献综述总结了63项研究,发现通气管植入前9个月期间提高了听力水平(A级)[1]。鼓膜通气管在位时可有明确的听力获益,但脱管后并没有显示出持久的疗效(A级)[1]。因此儿童复发性OME第一次脱管后需要重新植入通气管,可使用长期植入的通气管或进行腺样体切除术以获得更持久的疗效。
反复发作的急性中耳炎是鼓膜通气管植入的另一个指证。因为其分类困难且缺乏高质量的临床研究,临床上更加难以精确评估。事实上,复发性急性中耳炎(AOM)可伴有或不伴有积液。目前还不清楚是否以及如何区分慢性OME合并复发性AOM和AOM后中耳积液。无论如何,许多前瞻性研究已经表明,鼓膜置管对持续存在的复发性AOM伴中耳积液有效,有通气管时AOM发生频率明显降低(A级)[1]。另一方面,反复AOM发作的患儿,可在两次感染之间恢复干耳,这种情况下鼓膜通气管植入并不能使患儿获益。与美国版的指南观点一致,即不伴中耳积液的反复发作性中耳炎无需植入鼓膜通气管。
辅助腺样体切除术除了鼓膜置管术,腺样体切除术也可增加OME手术的疗效。最近的Meta分析已经得出结论,腺样体切除术的临床疗效获益至少有两年(A级)[1]。另一项前瞻性研究也证实腺样体切除术使得植入短期通气管后听力改善疗效延长了两年(A级)[1]。一项大型前瞻性研究还发现腺样体切除术降低了OME复发需要更换通气管的风险,特别是4岁以上的儿童(A级)[1]。
因此,大部分指南建议对4岁以上OME患儿进行腺样体切除术,通常作为鼓膜置管或鼓膜切开术的辅助治疗。美国儿童OME指南推荐腺样体切除术不作为4岁以下分泌性中耳炎儿童手术治疗的首选方案,因为其疗效有限,且临床意义尚有争议。如果有明确的指征,如慢性腺样体炎和鼻塞(由于腺样体肥大引起的),腺样体切除术也可以和鼓膜置管术同时进行。对于更小的年龄,问题则更复杂。这个年龄段的患儿临床获益似乎很差(原因尚不清楚)。由于可能出现的一些罕见的手术风险,并不推荐腺样体切除术。考虑到腺样体切除术的长期获益,复发性OME患者可在植入鼓膜通气管同时行腺样体切除术。
结论
此次共识在OME诊疗的主要问题上达成了一致,包括初始评估,以及药物和手术治疗。首先,需要对儿童进行彻底的检查以确定是否需要进行GERD和过敏的进一步评估。在大多数情况下,如果孩子没有任何不正常的病史,唯一建议的测试是一个适合年龄的听觉测试,应该在鼓膜置管之前完成。除了咽鼓管吹张之外,非手术治疗很难解决因年龄造成的咽鼓管功能障碍。不推荐使用糖皮质激素(口服或鼻内)、抗生素、减充血剂或抗组胺药治疗OME。目前国内治疗儿童OME的现状尚有待改进,在评估GERD和过敏方面缺乏足够的认识,往往忽视了可能存在的潜在病因。在药物治疗方面,糖皮质激素在缺乏足够证据支持的情况下被广泛使用,增加了医疗成本的同时也带来了副作用,且收效甚微。关于手术,鼓膜置管术应根据儿童进行个体化治疗。通气管有助于改善听力,并减少复发性AOM形成积液的机会。所以对儿童OME患者而言,鼓膜置管是一种恰当的治疗方式。在复发性OME中,伴有鼻塞或年龄较大的儿童,应考虑同时行腺样体切除术,可延长通风管植入的疗效。
[1]SimonF,HaggardM,RosenfeldRM,etal.Internationalconsensus(ICON)onmanagementofotitismediawitheffusioninchildren.EurAnnOtorhinolaryngolHeadNeckDis.Feb;(1S):S33-S39.
来源:刘宇鹏,杨军。◆儿童分泌性中耳炎治疗国际共识(IFOS)解读及国内诊疗现状。
◆临床耳鼻咽喉头颈外科杂志。
◆.32(21):-
温馨提示
《ENT界》作为《ENT联盟》服务号的兄弟订阅号,协同整合耳鼻咽喉头颈等学科资源,丰富该学科资讯,为耳鼻咽喉头颈及相关学科医患提供网络资料信息支持,为耳鼻咽喉领域提供新媒体互动及推广服务。
预览时标签不可点收录于话题#个上一篇下一篇转载请注明:http://www.zenmeshoutui.com/jbyh/8953.html